EDGC의 다양한 최근 보도자료를 확인하실 수 있습니다.
EDGC-EDGC헬스케어, 코로나19 진단시약 유럽 수출 계약 체결
등록일 : 20-03-19 16:51 조회수 : 6,725

글로벌 유전체 정밀의학기업 이원다이애그노믹스(이하 EDGC)는 계열사인 EDGC헬스케어가 관계회사 솔젠트의 코로나19 진단시약 유럽 수출 계약을 체결했다고 19일 밝혔다.
EDGC는 체외진단 의료기기 계열사인 EDGC헬스케어가 유럽대형 검진센터인 신랩(Synlab Holding GmbH, 이하 SYNLAB)과 3만 명 분의 코로나19 진단시약 수출 계약을 체결했다고 밝혔다. 지난 주 이미 진단시약 테스트를 SYNLAB이 현지에서 진행한 뒤 적합 판정을 받았으며 금주 초도 3만 명 분의 물량에 이어 다음 주부터 매주 점차 물량을 늘려 대규모의 시약 공급을 진행한다고 밝혔다.
SYNLAB은 독일에 본사를 둔 글로벌 검진센터로 2017년 기준 연간 매출액 약 19억유로(약 2조 6천억원)에 달해 유럽 내 검진센터 중 검진 규모 1~3위를 차지하는 글로벌 검진센터다. 현재 유럽 34개국과 일부 중동 및 남미 지역에 8개국을 포함하여 총 42개 지사를 운영하고 있는 SYNLAB은 대학병원을 비롯한 종합병원과 소규모 검진센터 등 다수의 의료기관을 대상으로 연간 약 5억 건 이상의 진단 검사 서비스를 제공하고 있다.
EDGC 헬스케어 이명희 대표이사는 "관계회사인 솔젠트의 코로나19 진단 시약이 유럽인증(CE)을 이미 받은 만큼 유럽 국가에서 다수의 계약 문의가 들어오고 있다"며 "급박한 세계적 상황에 따라 EDGC가 보유한 글로벌 네트워크를 통해 솔젠트의 코로나19 진단시약 보급이 필요한 국가에 빠르게 공급될 수 있도록 최선을 다하겠다"고 밝혔다.
한편, 의약품이 수출되려면 먼저 식품의약품안전처로부터 수출용 허가를 받는 등 승인 과정을 밟아야 하며, 이후 각 수출국 허가 당국의 규정에 따라 최종 승인을 받아야 정식으로 해당 국가 내 판매가 가능하다. 솔젠트의 코로나19 진단시약은 식약처 승인 및 CE를 모두 획득하고 있어 유럽 국가에 수출 계약 및 공급이 가능하다. 질본 긴급사용승인을 받은 4개 업체 중 직접 개발 및 생산한 핵심원재료로 코로나19 진단시약을 생산하는 업체는 솔젠트가 유일하며 자체 기술력과 노하우를 국제 표준인 ISO 9001, ISO 13485 및 우수제조관리기준인 KGMP 등 품질경영에 접목시켜 코로나19 진단시약을 생산하고 있다.
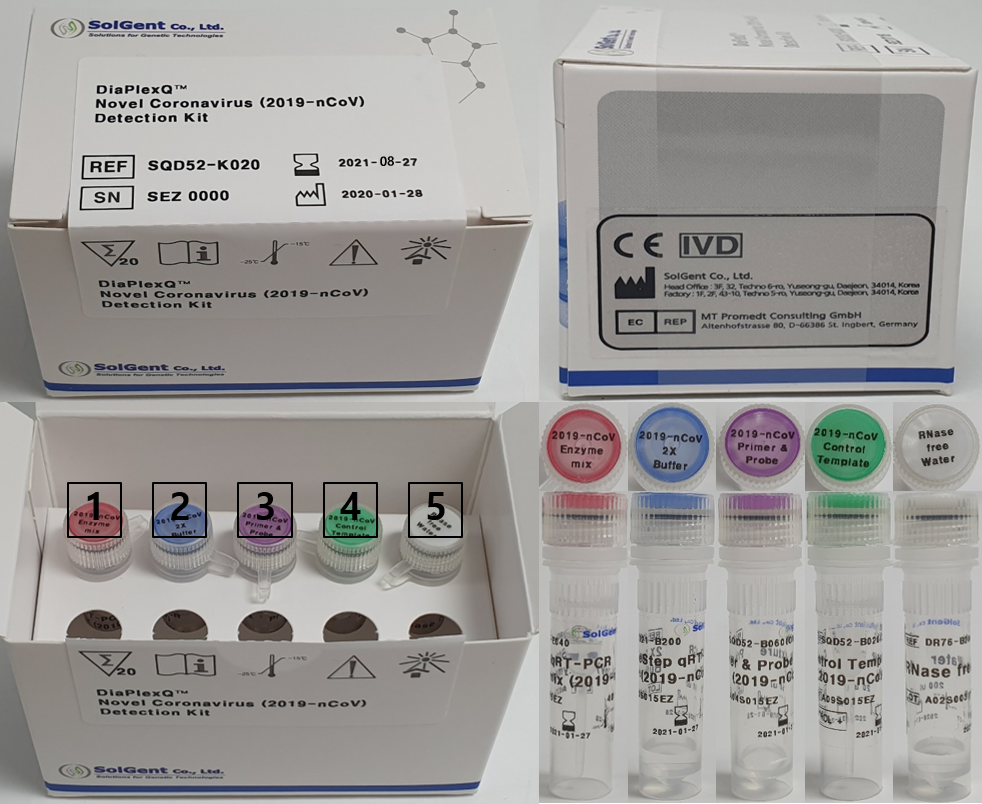
[DiaPlexQ™ Novel Coronavirus (2019-nCoV) Detection Kit, 솔젠트]